人工智能在生物医药和生物材料设计中的赋能作用至关重要,通过先进的模型算法和数据分析,能深入解析药物分子的构效关系,优化候选药物结构,极大地缩短研发周期并降低成本。但聚合物不确定的序列和复杂的分子组成使其难以全面表征结构,且生物活性聚合物的样本量小,难以构建大数据模型进行精准预测。因此,如何基于人工智能实现小样本数据下聚合物结构预测是领域核心挑战,对促进药物研发的自动化、智能化有着重要研究意义,也是国际研究的热点与前沿。
近日,华东理工大学金沙集团1862cc成色唐漾教授与材料学院刘润辉教授在人工智能和抗耐药菌多肽模拟聚合物进行跨领域合作研究。首次在基于人工智能实现小样本多肽模拟聚合物活性预测和逆向设计研究中取得关键突破,仅依赖小样本(<100)结构与活性数据实现在庞大聚合物空间(>1060)中精准预测聚合物抗菌活性,并通过逆向设计发现大量具有突出广谱抗耐药菌活性和高选择性的优选聚合物结构,为抗耐药菌多肽模拟聚合物研究提供了新思路。该成果以“AI-guided Few-shot Inverse Design of HDP-Mimicking Polymers against Drug-Resistant Bacteria”(人工智能辅助抗耐药菌宿主防御肽模拟聚合物的小样本逆向设计)为题发表在Nature Communications 《自然•通讯》上(https://www.nature.com/articles/s41467-024-50533-4)。
全球抗生素耐药性风险不断升级,亟需探索高效抗耐药菌广谱抗菌剂的新策略。宿主防御肽(HDP)因具有抗耐药菌活性和不易使微生物产生耐药性等优势被寄予厚望,但易结构不稳定、易酶解、难以大规模制备等缺点限制其实际应用。但传统半经验化的设计方法仍难以满足抗耐药菌化合物的迫切需求。尽管人工智能辅助药物发现研究已经取得进展,但多肽模拟聚合物的无规序列使得难以通过计算机信息全面表征聚合物结构,且小样本数据限制了对聚合物性能的精准预测与对超高维聚合物空间的高效探索。因此,基于小样本聚合物实现人工智能设计具有理想目标活性的优选聚合物一直未取得突破,距离理想人工智能驱动下实现药物设计的自动化仍旧任重而道远。
前期,唐漾教授等就小样本学习与多模态表征学习开展相关研究,聚焦提高小样本数据下模型的预测性能,为本研究打下良好基础。刘润辉教授课题组通过多肽聚合物模拟宿主防御肽实现了体内外高效抗耐药菌活性,显示了多肽聚合物在抗耐药菌研究中的广阔前景,为聚合物合成与验证提供坚实的技术支撑(IEEE/ACM Trans. Comput. Biol. Bioinf. 2023, 20, 3044-3055;IEEE/CAA JAS. 2023, 11, 1106-1126;Nat. Microbiol. 2024, 9, 1325;Nat. Commun. 2021, 12, 5898;Nat. Commun. 2018, 9, 5297;J. Am. Chem. Soc. 2023, 145, 25753;J. Am. Chem. Soc. 2022, 144, 1690;Angew. Chem. Int. Ed. 2020, 59, 7240)。
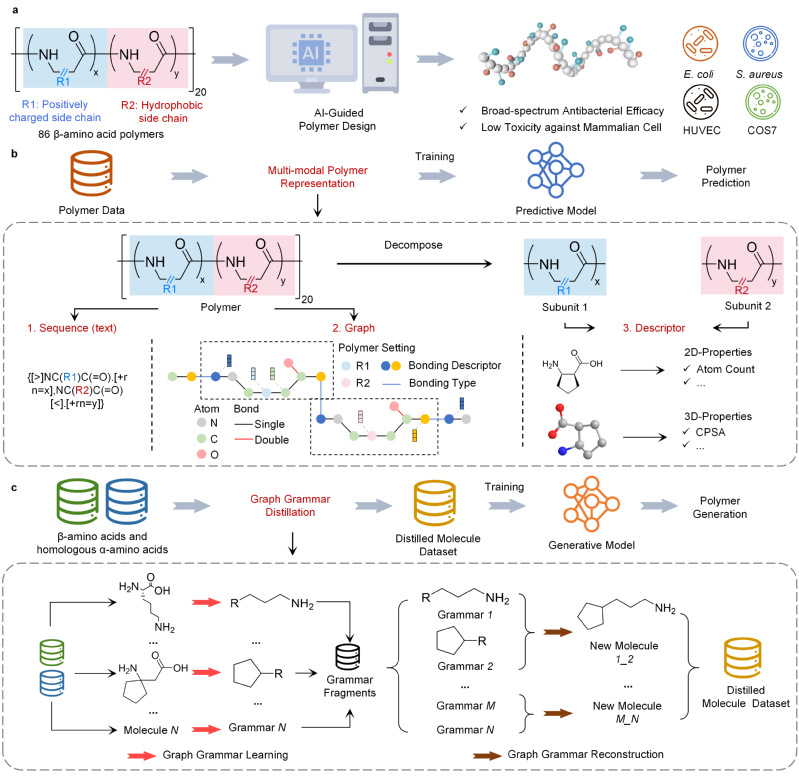
图 基于小样本β-多肽聚合物的人工智能框架实现聚合物逆向设计
本研究以β-多肽聚合物为模型,通过构建面向聚合物的多模态信息(文本序列、图形、描述符)表征构架以提取完整、全面的多尺度聚合物信息训练预测模型,实现小样本聚合物数据下对海量聚合物结构的精准抗菌性能预测。通过搭建图语法蒸馏框架,将β-氨基酸与同源天然的α-氨基酸的化学结构拆解为大量分子图语法片段,并重新组合成新的分子以训练生成模型,实现小样本数据精准定位高维聚合物空间的搜索范围,通过强化学习实现预测模型与生成模型的迭代交互,获得83个具有广谱抗耐药菌活性和高选择性的优选聚合物库。最后对其中一个优选聚合物DM0.8iPen0.2开展合成与抗耐药菌研究,结果表明人工智能模型预测抗菌活性与实验数据高度一致,验证了人工智能对多肽模拟聚合物活性的精准预测,验证了人工智能驱动下的药物自动化设计的可行性。
金沙集团1862cc成色博士研究生吴天宇、材料科学与工程学院副研究员周敏是论文的第一作者,材料科学与工程学院刘润辉教授和金沙集团1862cc成色唐漾教授为通讯作者。本论文得到了中国工程院院士钱锋教授和欧洲科学院院士Jürgen Kurths教授的悉心指导。该成果得到了国家自然科学基金委基础科学中心项目、国家自然科学基金委杰出青年基金项目、国家自然科学基金委重点项目、科技部重点研发计划项目等课题的资助。


